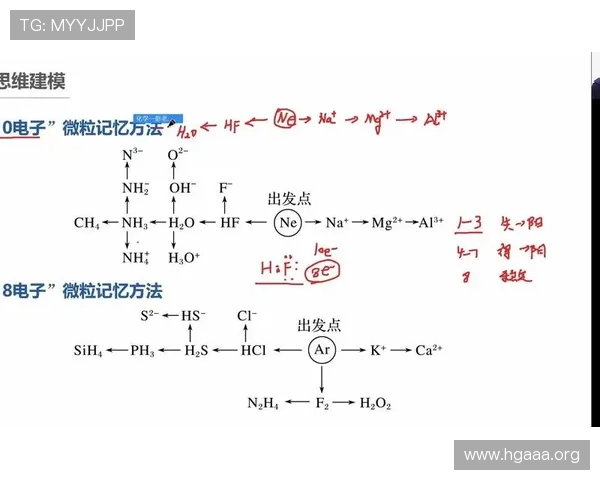
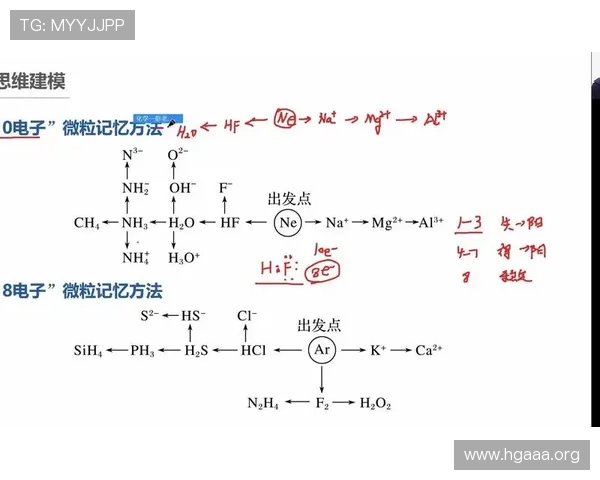
18电子规则的意义及其在化学结构中的重要作用
了解18电子规则的基本概念
18电子规则简介
18电子规则是化学中描述过渡金属配合物稳定性的重要原则之一。它指出,稳定的过渡金属配合物通常拥有恰好18个价电子,类似于稀有气体的电子排布。这一规则最早由化学家诺贝尔奖获得者吉尔伯特·路易斯提出,旨在帮助理解金属配合物的稳定性和反应性。
电子数的计算方法
在应用18电子规则时,电子数的计算包括金属中心的价电子数和配体提供的电子数。具体计算方式如下:
| 组成部分 | 电子数计算 | 说明 |
|---|---|---|
| 金属中心 | 根据元素原子序数确定 | 例如,铁(Fe)为26号元素,通常以Fe(0)或Fe(II)状态考虑 |
| 配体电子 | 根据配体类型确定 | 配体如氨(NH₃)提供2电子,乙烯(C₂H₄)提供2电子 |
通过合理计算,判断配合物是否趋向于稳定。
18电子规则在化学结构中的应用
配合物的稳定性预测
18电子规则广泛应用于过渡金属配合物的稳定性预测。例如,铁、钴、镍等元素的配合物中,达到18电子的结构通常表现出较高的稳定性。这一规律帮助化学家设计新型配合物,优化其性能。
典型的18电子配合物
一些经典的18电子配合物包括:
- Ni(CO)₄:镍四羰基,电子总数为18,结构稳定。
- Fe(CO)₅:五羰基铁,电子数为18,具有良好的稳定性。
- Co(CO)₃(PPh₃):三羰基三苯基膦钴,电子数达到18,表现出优异的化学稳定性。
这些配合物在催化、材料科学等领域具有重要应用。
电子数偏离18的影响
当配合物的电子数偏离18时,通常表现出不同的化学性质。例如,电子数少于18的配合物可能更具反应性,易于发生配位或还原反应;而电子数超过18的配合物则可能表现出较高的稳定性或特殊的反应路径。
18电子规则的局限性与发展
规则的适用范围
18电子规则主要适用于强场配体和特定过渡金属的配合物,对于一些特殊体系或弱场配体,规则的适用性有限。例如,某些稀有金属或特殊配体体系中,电子数可能偏离18,但配合物仍然表现出稳定性。
现代研究的拓展
随着化学研究的深入,科学家不断扩展和修正18电子规则。例如,某些配合物表现出“超18电子”状态,电子数超过18,但仍具有稳定性。这推动了对电子结构和配合物稳定性理解的不断深化。
18电子规则在化学结构设计中的意义
| 作用领域 | 具体应用 | 重要性 |
|---|---|---|
| 催化剂设计 | 设计高效催化剂 | 提高反应效率和选择性 |
| 材料科学 | 合成新型功能材料 | 改善材料性能 |
| 药物开发 | 制备药用配合物 | 提升药效和稳定性 |
合理利用18电子规则,有助于科学家在设计新材料和新药时实现目标,推动化学工业的创新发展。
结论总结
18电子规则作为理解过渡金属配合物稳定性的重要工具,为化学研究提供了理论基础。它不仅帮助预测配合物的稳定性,还指导新材料和催化剂的设计。尽管存在一定的局限性,但随着研究的不断深入,规则的应用范围逐渐扩大,推动了现代化学的发展。
作者点评
18电子规则在化学结构中的应用具有深远意义。它不仅是理解过渡金属配合物稳定性的基础,也为新材料的设计提供了理论指导。未来,随着电子结构研究的不断深入,规则的完善和拓展将带来更多创新的可能性,为化学行业带来更多突破。
常见问题解答
1. 18电子规则的起源和发展背景是什么?
18电子规则最早由吉尔伯特·路易斯提出,旨在解释过渡金属配合物的稳定性。随着化学研究的深入,科学家逐步发现许多配合物符合这一规则,从而推动了其广泛应用。近年来,研究者不断修正和扩展这一规则,尤其是在超18电子配合物的发现中,推动了电子结构理论的发展。
电子数的计算主要包括金属中心的价电子数和配体提供的电子数。具体步骤如世界杯网站app官网下:
- 确定金属的氧化态和电子配置;
- 根据配体类型计算提供的电子数;
- 将两者相加,判断是否达到18电子。
例如,钯(Pd)在+2氧化态时,电子数为(46-2=44),配合物中配体提供电子后,计算总电子数。
3. 18电子规则适用于哪些类型的配合物?
主要适用于过渡金属的强场配合物,尤其是那些具有较强配体场的体系,如羰基、氨、烯等配体。对于稀有金属或弱场配体,规则的适用性较低,可能需要结合其他理论进行分析。
4. 电子数偏离18会带来哪些影响?
偏离18电子数的配合物可能表现出不同的化学性质。例如,电子数少于18的配合物通常反应性更强,易发生配位或还原反应;而电子数超过18的配合物则可能具有较高的稳定性或特殊的反应路径。这些差异对于催化剂设计和反应调控具有重要意义。
5. 现代科学如何扩展和修正18电子规则?
随着电子结构研究的深入,科学家发现一些配合物表现出“超18电子”状态,电子数超过18但仍稳定。这推动了对电子云分布、轨道重叠等因素的研究,促使规则不断完善,以适应复杂体系的需要。
6. 18电子规则在催化剂设计中的具体应用有哪些?
在催化剂设计中,科学家通过调节配体类型和金属氧化态,使配合物达到18电子,从而提高催化效率。例如,利用18电子配合物作为催化剂,可以实现高选择性和高效率的反应,广泛应用于有机合成和工业催化。
7. 电子数偏离18的配合物是否都不稳定?
不一定。虽然18电子配合物通常较为稳定,但某些偏离的配合物也可以表现出稳定性,尤其是在特殊电子环境或特殊配体的作用下。例如,超18电子配合物在某些反应中具有特殊的催化性能。
8. 18电子规则在新材料开发中的作用是什么?
在新材料开发中,科学家利用18电子规则设计具有特定电子结构的配合物,以实现优异的性能。例如,开发高强度的金属-有机框架材料或新型催化剂,均依赖于对电子数的合理控制。
9. 未来18电子规则的发展趋势如何?
未来,随着电子结构理论和计算化学的发展,18电子规则将不断完善,可能结合量子化学等先进技术,提供更精准的配合物稳定性预测模型。同时,超18电子和非经典电子配置的研究也将成为热点。
10. 如何利用18电子规则进行配合物的设计?
设计配合物时,首先确定金属的氧化态和电子数,然后选择合适的配体以达到18电子的目标。结合计算模拟,可以优化配体类型和配比,从而获得稳定且性能优异的配合物。这一过程在催化剂和新材料开发中尤为重要。
内容总结
本文详细介绍了18电子规则的基本概念、计算方法及其在化学结构中的应用。通过对典型配合物的分析,阐释了电子数对配合物稳定性的重要影响。尽管存在一定局限性,随着研究的不断深入,18电子规则在现代化学中的地位愈发重要,为新材料设计和催化剂开发提供了理论基础。
作者认为,18电子规则不仅是理解过渡金属配合物的基础工具,更是推动化学创新的重要动力。未来,结合先进的电子结构分析技术,规则的应用范围将不断扩大,为化学科学带来更多突破。
关键词
18电子规则、过渡金属配合物、电子数计算、配合物稳定性、催化剂设计、超18电子、化学结构、配体作用、电子结构理论、材料科学